癌症为何多年后卷土重来?
2026-04-04 11:25:15 · chineseheadlinenews.com · 来源: 自然系列
研究人员正瞄准那些处于休眠状态的肿瘤细胞,这些细胞或许能解释为何某些癌症在成功治疗多年后又会复发。
2017年,Lisa Dutton被宣布乳腺癌痊愈了。她与亲友们欢庆了一番,但她知道,抗癌之路未必就此结束。据统计,在经治疗清除乳腺肿瘤的患者中,多达三分之一的人会面临癌症复发,有时甚至发生在数十年后。已知许多其他癌症也会在初次治疗后的数年内复发,有些部分复发率甚至更高。
“这个念头始终萦绕心底,带来无形的压力。”现居宾夕法尼亚州费城的退休医疗管理顾问Dutton说。
作为治疗方案的一部分,Dutton参与了一项名为SURMOUNT的临床试验。该试验将监测她体内可能存在的休眠癌细胞——许多研究者现在认为,这至少能解释部分癌症的复发[1]。这些休眠的肿瘤细胞躲过初期治疗,迁移至身体其他部位。与典型转移性癌细胞(从原发肿瘤扩散)立即增殖形成新肿瘤不同,休眠细胞会持续“沉睡”。它们躲避免疫系统的侦察,也暂停活跃分裂。然而在未来的某个时刻,它们可能被重新激活,引发肿瘤。
尽管Dutton明白治疗可能未能清除所有癌症迹象,但2020年第一次在骨髓中发现休眠细胞时,她仍感到如遭重创。
研究人员正逐渐在乳腺癌、前列腺癌、肺癌、结直肠癌等多种癌症中发现此类休眠肿瘤细胞(亦称播散性癌细胞)[2],它们与部分转移性癌症之间的关联愈发显著。据估计,约30%经成功治疗的癌症患者体内可能潜藏着这些细胞,而尚未发表的研究数据显示其实际存在可能更为普遍。
图源:pixabay
过去十年间,科学界掀起了识别与研究休眠细胞的热潮,终极目标是开发针对性疗法。目前已有数项临床试验正在进行,旨在验证潜在治疗策略的有效性。
尽管Dutton起初参与的试验仅监测细胞动态,但她后来又加入了名为“CLEVER”的另一项试验,目标是清除这些休眠细胞[3]。随着此类试验持续推进,关于“沉睡细胞”的诸多未解之谜(包括其休眠诱因及应对策略),正吸引着更多研究者投身这一领域。
美国弗雷德·哈钦森癌症中心的癌症生物学家Cyrus Ghajar说,“我们开始看到多个研究团队提出相同理念,这总是非常鼓舞人心的。”当前开展的试验“恰印证了该领域取得的巨大进展”。
潜伏的威胁
早在20世纪30年代就有人提出了休眠肿瘤细胞的存在。当时,澳大利亚病理学家Rupert Willis将某些继发性癌灶归因于这类细胞[4]。随着癌症治疗后的患者生存期延长,他与其他学者注意到,疾病有时会在多年后卷土重来,且往往更具侵袭性。尽管这一假说提出甚早,休眠理论在随后数十年间并未被广泛接受。
宾夕法尼亚大学医生科学家Lewis Chodosh回忆道,二十多年前他与同行探讨这一想法时曾遭遇诸多反对。他表示,当时无人愿意相信抗癌药物还会留下残余,制药公司也对为“已治愈”患者开发疗法兴趣寥寥。当时许多科学家说复发性癌症应是全新病变,与既往诊断无关。
“只有证据积累到足够多,才能走出这个思维方式。”Chodosh说。他与宾夕法尼亚大学佩雷尔曼医学院肿瘤内科学专家Angela DeMichele共同担任SURMOUNT与CLEVER研究的联合负责人。

Angela DeMichele(左)与Lewis Chodosh正致力于研究靶向休眠肿瘤细胞的方法。图片来源:Penn Medicine/Peggy Peterson
通过使用几种细胞标记物,研究人员如今已能在身体多个部位识别出休眠肿瘤细胞[5]。这些标记物不仅能帮助科学家判断细胞是否处于生长分裂状态,还能追溯其起源部位,进而确定它们与何种癌症相关。然而,现有方法并非完美,研究人员仍在努力确定是否某些细胞比其他细胞更容易进入休眠状态,以及什么是界定这类细胞的关键特征。
Ghajar等学者研究发现,在癌症进展早期,休眠细胞就已脱离原发肿瘤,通常在疾病被确诊之前[6]。至于这些细胞如何及为何脱离尚不完全明确,但它们在循环系统中仅停留数分钟后,便会离开血流,聚集于骨髓与淋巴结等特定部位。Ghajar指出,即便在这些特定微环境中,休眠细胞也极为稀少,数百万健康细胞中仅有几个。休眠细胞生命活动停滞的状态,使其能躲避针对快速分裂细胞的传统疗法,如化疗。
休眠状态与其他已知状态如细胞衰老不同,衰老是细胞在死亡前停止分裂的自然过程。瑞士日内瓦大学肿瘤内科医生Petros Tsantoulis表示,休眠的、与肿瘤有关的细胞衰老和静止状态尚未得到明确定义,科学家仍在试图厘清这些差异。
我们已经知道的是,在适当条件下,休眠细胞能重新启动分裂程序。一旦苏醒,这些细胞会增殖形成肿瘤,并完整复现原发肿瘤的复杂特性。
这一发现促使部分研究者提出:休眠肿瘤细胞可能就是所谓的癌症干细胞,这类细胞通过自我更新与分化能力催生肿瘤;或至少,它们可能是具有类似干细胞特征的癌细胞。
休眠肿瘤细胞具有某些通常与干细胞相关的特征,例如特定基因的过表达。纽约斯隆·凯特琳研究所所长、癌症生物学家Joan Massagué指出,干细胞大部分时间处于休眠状态,仅在损伤或疾病发生后才会被激活——这使它们成为休眠癌细胞研究的理想参照模型。不过,癌症干细胞的存在本身仍是个有争议的概念。
科学家们似乎即将解答一些未决的问题。随着先进实验技术使研究者能够更密切地观测单个细胞,如今已可识别、分离并富集休眠肿瘤细胞以供深入研究。例如,Chodosh和DeMichele的团队正在开发一种鉴定休眠细胞的检测方法。Chodosh表示,该方法灵敏度远高于现有技术,或能更精准评估休眠细胞的携带人群有多少。
与此同时,Ghajar正建立起一种新的方式来理解这些细胞。例如,若一个来自乳腺肿瘤的休眠细胞后来进入骨髓,人们通常预期它会保留乳腺癌细胞的诸多特征以便识别。“但我们发现实际情况往往不同。”Ghajar指出,癌细胞一旦扩散,其形态、大小和行为常会发生改变。“我们必须超越基于统一特征的定义方式,转而通过比对这些细胞与原始肿瘤的突变来界定——不是依狙桃们设想它应如何,而是根据基因组信息来定义播散性癌细胞。”
沉睡与苏醒的信号
除了界定休眠状态,研究者更希望探明细胞如何及为何进入休眠,以及哪些因素会使它们重新活跃起来。
美国丹娜-法伯癌症研究所的免疫学家Judith Agudo认为,细胞进入休眠很可能是一种自我保护机制。她解释道,在肿瘤内部,单个细胞或许能免受免疫系统攻击,但一旦脱离集体后,“若不采取隐蔽措施,就很容易被清除”。此外,细胞在体内迁移到新位置的过程充满压力,绝大多数脱离的细胞会在此过程中死亡。休眠是适应恶劣环境的一种生存方式。
研究表明,细胞在休眠期间仍会与其微环境持续对话[7],并通过自我调整主动维持休眠状态。例如,休眠细胞似乎会改变涉及细胞存活的基因表达模式,包括一个称为mTOR通路的核心代谢与生长调控枢纽[8]。这些细胞还利用一种名为自噬的自我循环机制,使休眠细胞能够重新利用内部资源,在极少外界供给的情况下维持生存[9]。
这些细胞与其外部环境(包括免疫系统)之间似乎也存在着错综复杂的互动。美国蒙特菲尔-爱因斯坦综合癌症中心癌症休眠研究所创始主任Julio Aguirre-Ghiso指出,免疫反应不仅参与诱导休眠,也涉及其维持与终结的过程。
他与团队的研究表明,肺部的巨噬细胞会产生一种特定蛋白质,该蛋白能与休眠的乳腺癌细胞结合并强化其休眠状态[10]。其他研究也揭示了休眠细胞如何逃避免疫系统细胞(包括T细胞[11]和自然杀伤细胞[12])的监测机制。
综合来看,这些研究表明细胞通常会保持休眠状态,直至免疫环境格局因某种原因被打破,使平衡发生足以让细胞“安全苏醒”的倾斜。这种转变可能由损伤或疾病引发,近年研究已将细胞损伤[13]、COVID-19感染及流感感染[14]与细胞脱离休眠状态联系起来。此外,衰老、纤维化[15]、慢性压力或生活方式选择亦可能成为重新激活的诱因。
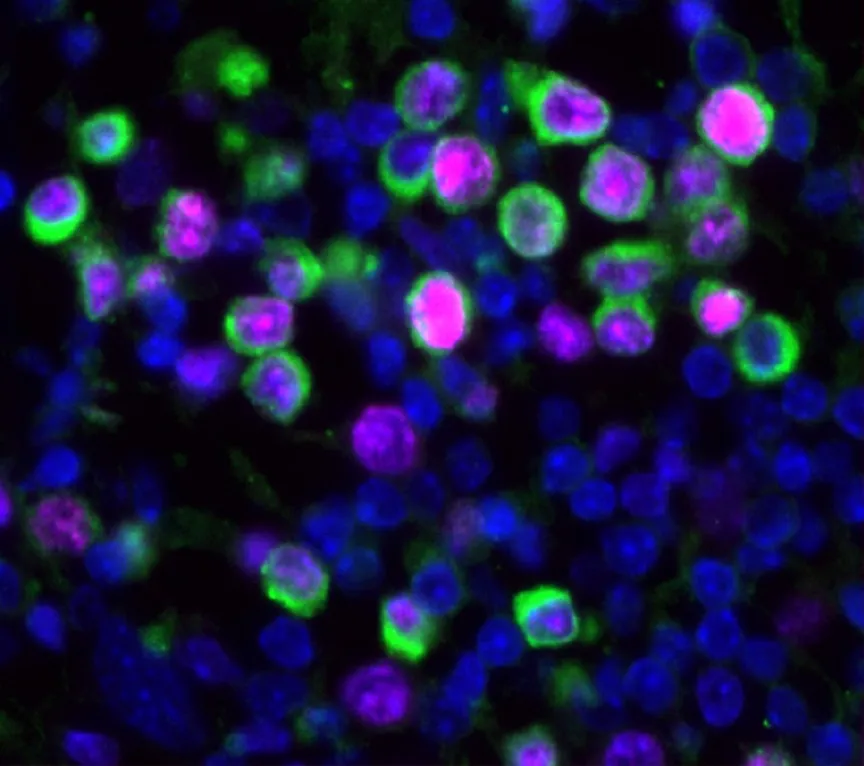
流感感染会迫使休眠肿瘤细胞(绿色)开始生长分裂。图片来源:Bryan Johnson
对于这些细胞而言,“这本质上是一场芭率的博弈。”美国塔夫茨大学生物医学工程师Shelly Peyton解释说。细胞在微小扰动后会不断尝试脱离休眠状态,却往往遭遇清除。“但当平衡被打破时,癌症转移往往就此爆发。”
Peyton的研究聚焦于纤维化——即受损部位纤维结缔组织的异常增生。这种现象常与癌症相关,因为组织硬化会促进肿瘤生长并加强细胞间信号传递。但休眠细胞常驻的骨髓环境本身柔软,Peyton关注这种柔软特性是否正是维持休眠的关键因素之一。她指出,自然的年龄相关性骨密度下降(骨质疏松),或曾患乳腺癌女性的激素变化,都有可能触发纤维化,并可能唤醒癌细胞。
没有单一的方法
2018年,当美国食品药品监督管理局(FDA)将癌症疗法的范围扩展到不仅包括缩小肿瘤,还包括预防或延缓继发性肿瘤生长时,针对休眠细胞的治疗研发获得了监管层面的推动。目前大多数靶向休眠状态的研究团队,都致力于通过就地清除休眠细胞来预防此类复发。
一种策略是让休眠细胞暴露于巡游的免疫细胞视野中。例如Ghajar认为,休眠细胞之所以能隐藏,并非依靠某种精妙的免疫逃逸机制,而是因为接触它们的T细胞数量不足。他和他的团队正在研究,CAR-T细胞疗法(对患者自身免疫细胞进行基因改造)是否能够提高免疫细胞与休眠肿瘤细胞的接触概率[16]。
另一些研究者则瞄准癌细胞赖以存活的信号传导与代谢通路。那些通过不依赖细胞分裂的机制来靶向活跃癌细胞的治疗方法,可能对休眠肿瘤细胞同样有效。
Aguirre-Ghiso专注于靶向允许细胞在恶劣环境中存活的通路,他指出活跃细胞与休眠细胞都依赖相似的机制持续出现在不该出现的地方。
他在纽约联合创立了一家名为HiberCell的公司,开发出一种能抑制PERK酶的分子。这种酶参与细胞在应激刺激后恢复稳定状态的过程,即“整合应激反应”。该PERK抑制剂通过适度破坏这种应激反应来实现细胞清除。
基于临床前期研究结果[17],FDA已对该抑制剂针对胃癌及其他实体瘤的治疗方案予以加速审批。研究团队于2023年完成了I期临床试验[18]。尽管该试验主要针对一般性的癌细胞,Aguirre-Ghiso表示,他们团队正在动物模型中研究该分子对肺部和骨髓内休眠肿瘤细胞的清除效果。
或许突破性的进展会源于阻断自噬作用的尝试——此举旨在限制休眠细胞的自我修复能力。“由于这类细胞维持存活所需资源极少,即使仅剥夺其微少资源,也足以将其推向死亡螺旋。”澳大利亚奥利维亚·纽顿-约翰癌症研究所的乳腺癌专家Robin Anderson说。
阻断自噬正是Dutton参与的CLEVER二期试验的目标,也是DeMichele与Chodosh所负责的另外两项研究的基础。这三项试验正在测试自噬抑制药物羟氯喹的单药疗效及联合疗法效果。联合方案包括干扰mTOR信号通路的药物、阻断细胞增殖的制剂,以及通过解除肿瘤伪装使其暴露于免疫系统的免疫疗法。
在CLEVER试验中,约50名乳腺癌患者接受了羟氯喹单药或联合mTOR抑制剂依维莫司的治疗[3]。仅接受羟氯喹或依维莫司单药治疗的患者,其休眠肿瘤细胞有所减少,而联合疗法的效果更为显著。研究显示,经6至12个月联合治疗后,87%的参与者体内潜伏的休眠肿瘤细胞被清除。
DeMichele说,目标是在开展试验前先确定一种理想的药物组合。尽管她在自噬抑制研究上全力推进,但也强调休眠难题不可能仅靠单一方法解决。随着对休眠机制认知的深入及其复杂性的日益显现,多种疗法正在同步探索中。“未来我们或将拥有更丰富的治疗工具箱,可根据患者具体情况灵活选择。” DeMichele说。
SURMOUNT监测试验已获得延长资助,现年六十余岁的Dutton同意接受未来20年的持续监测。她表示,自己的参与既有助于研究人员理解这些细胞,同时也让她感到安心。
“掌握信息对我很重要。”她说,“知道正在发生什么,让我感到自己正在为争取良好预后竭尽所能。”