肾透明细胞癌诊疗一体化研究取得重大突破
2026-03-08 01:25:15 · chineseheadlinenews.com · 来源: 中国科学报
肾透明细胞癌(ccRCC)的诊疗长期面临复发转移率高、传统影像学诊断和全身分期手段存在局限等棘手问题。近日,南方医科大学南方医院教授胡孔珍团队联合北京大学深圳医院教授赵永胜/陈海波团队,在ccRCC诊疗一体化研究领域取得重大突破,成功开发出靶向碳酸酐酶IX(CAIX)的新型诊疗放射性配体对,为ccRCC的精准成像与靶向放疗带来新希望。相关成果在线发表于《化学工程期刊》。
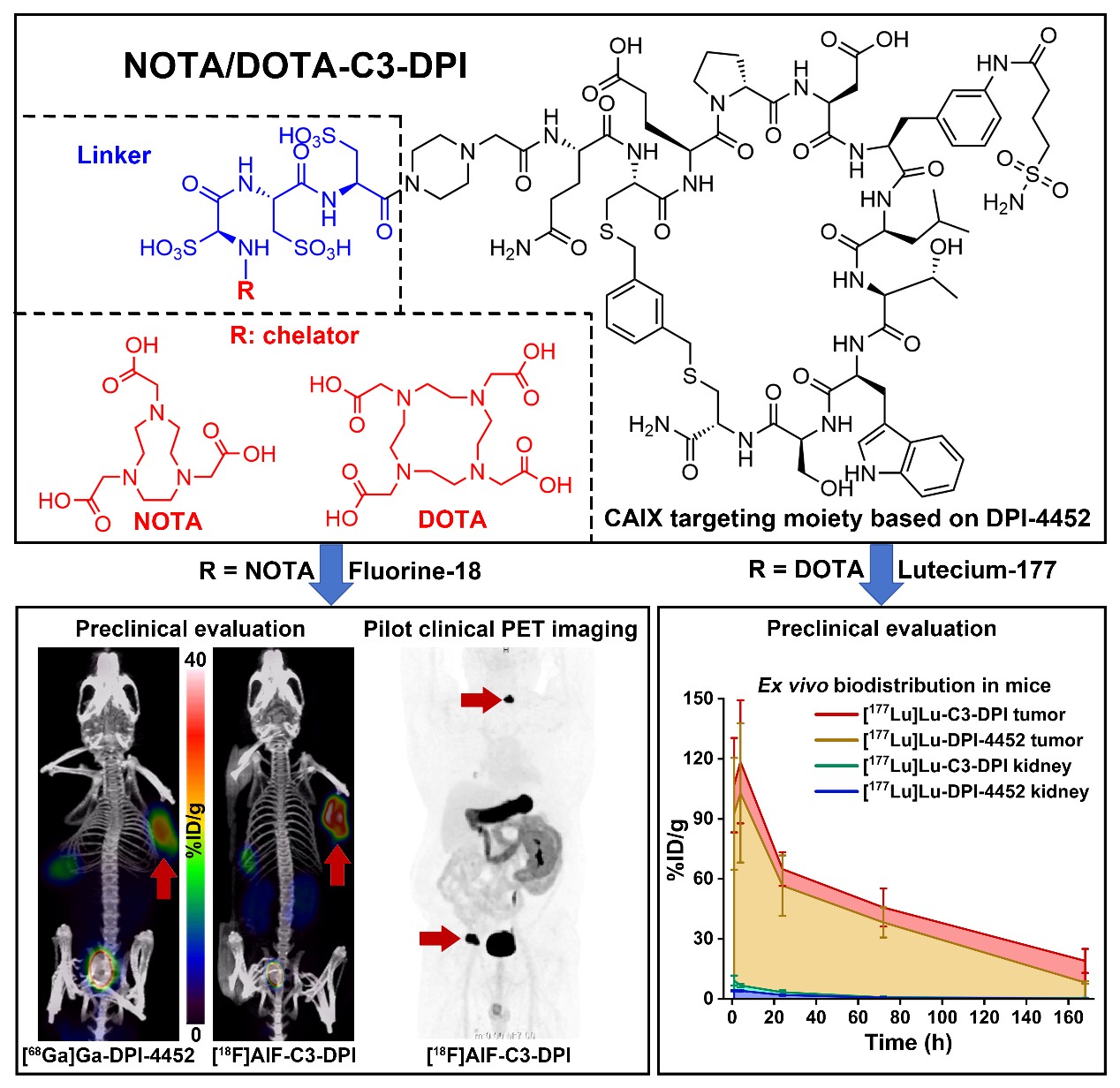
靶向CAIX的诊疗对([18F]AlF-C3-DPI/[177Lu]Lu-C3-DPI)可实现对ccRCC的精准成像与靶向放疗。研究团供图
肾细胞癌(RCC)全球每年新发病例约40万例,ccRCC占比极高。因其早期症状隐匿、易远处转移,传统影像学在早期精准定性诊断和全身精准分期上力不从心。放射性诊疗一体化作为新兴精准医学策略,通过相同或结构相似配体分别标记诊断与治疗核素,实现“诊断-治疗-疗效监测”闭环管理。CAIX在ccRCC中高度表达,是理想的放射性诊疗靶点,但此前报道的CAIX靶向探针存在肿瘤摄取不足、背景信号高、药代动力学不理想等问题。
针对这些难题,研究团队精心设计并合成了新型CAIX靶向配体NOTA-C3-DPI(用于PET成像)和DOTA-C3-DPI(用于内照射治疗)。论文通讯作者胡孔珍介绍:“我们通过分子结构优化,在配体结构中引入三磺基丙氨酸连接子,显著改善了体内药代动力学特性,从而实现ccRCC的精准成像与靶向放射治疗。”
在临床前评估阶段,两种配体对CAIX展现出纳摩尔级亲和力,且对其他碳酸酐酶亚型无明显抑制,高选择性特征突出。研究团队顺利完成了放射化学合成,[18F]AlF-C3-DPI可通过自动化模块大批量生产,为临床应用奠定基础;[177Lu]Lu-C3-DPI也成功标记且具有高比活度。
得益于三磺基丙氨酸连接子的引入,新型CAIX靶向诊疗的优势尽显。在体外表征中,其稳定性、靶点结合能力以及潜在肿瘤滞留能力等与已知示踪剂相当甚至更优;临床前生物学评估中更是表现卓越。[18F]AlF-C3-DPI的肿瘤摄取与滞留能力较已报道示踪剂显著提升,背景器官摄取包低;[177Lu]Lu-C3-DPI可有效抑制肿瘤生长,且安全性良好。
基于良好的临床前结果,研究团队将[18F]AlF-C3-DPI推进至初步临床转化研究。研究入组7例患者,包括6例ccRCC和1例乳头状RCC。注射后1小时进行PET/CT显像,4例患者同时行[18F]FDG PET/CT作为对照。
结果显示,在术后复发ccRCC患者中,[18F]AlF-C3-DPI清晰呈现多处远处转移灶,如脑、心包、肺静脉和骨转移,而常规传统影像技术未能明确识别。在广泛转移ccRCC患者中,[18F]AlF-C3-DPI清晰显示原发灶、癌栓及多处淋巴结和远处转移,常规[18F]FDG却呈假阴性。定量分析表明,[18F]AlF-C3-DPI在原发灶和转移灶中的摄取均显著高于[18F]FDG。此外,乳头状RCC患者对[18F]AlF-C3-DPI无摄取,进一步证实其对ccRCC的高度特异性。
该研究不仅提供了新的CAIX靶向诊疗对的分子设计与优化策略,更为ccRCC的精准分期、转移灶监测及靶向放射治疗搭建了全新的诊疗一体化平台,有力推动了核医学在肾癌领域的临床应用,为众多ccRCC患者带来新的治疗曙光。